
洗車キャンペーン!開催中 是非この機会にレンタル純水器を
初めての方にも手軽に純水洗車を体験していただける「レンタル純水器」をご提供しています
BLOG & INFO
私たちの生活に欠かせない水の質を改善するための手法の一つがイオン交換です。この技術は、樹脂の内部に保存されたイオンと水中に存在する他のイオンが互いに交換し合うことで成り立っています。例えば、イオン交換樹脂を使用して硬水を軟水に変える過程でのカルシウムイオンとナトリウムイオンの交換は、科学的に可逆的な反応であり、条件次第でそのバランスが変化します。
このようにこの記事では、イオン交換の基本的なメカニズムをはじめ、官能基の種類や代表的なイオン交換反応、さらに実際の応用例に至るまでを幅広く解説していきます。
イオン交換とは、ある種のイオンが別のイオンと交換される化学反応であり、このためにイオンを交換する樹脂つまりイオン交換樹脂、主に水処理や化学分析などに利用されます。この反応において、樹脂内部に固定されたイオンが水溶液中のイオンと置き換わることで、電荷のバランスが常に保たれるという特性が存在します。
具体的には、硬水中のカルシウムイオンがナトリウムイオンと交換されることによって水の硬度を下げることができ、これが家庭用の浄水器やボイラーにおける重要な機能となっています。
イオン交換反応は、可逆的なプロセスで、条件によっては平衡状態(イオン交換樹脂に吸着したり脱着したりする状態が一定の割合で起こっている)に達することもあります。このように、イオン交換は、私たちの生活空間での水質管理において非常に重要な役割を果たしています。
イオン交換の基本的なメカニズムは、イオンが樹脂と水中のイオンとの間で定常的に交換されるという点にあります。イオン交換樹脂は、特定のイオンを吸着する特性を持った高分子材料です。イオン交換樹脂は、「カチオン交換樹脂」と「アニオン交換樹脂」の二つに大別されます。カチオン交換樹脂は正の電荷を持つイオンを交換し、アニオン交換樹脂は負の電荷を持つイオンを交換します。
この反応では、樹脂に吸着されたイオンは、適切な条件下で水中のイオンと適宜交換され、さらにこの交換には選択性があるために、使用目的に応じた選択的なイオン除去が可能となります。イオン交換交換には、イオンに対する選択性があることが重要となります。
イオン交換樹脂にはさまざまな種類があり、主にカチオン交換樹脂とアニオン交換樹脂に分けられます。カチオン交換樹脂の一例としては、スチレン-ジビニルベンゼン系樹脂が挙げられます。これらの樹脂は、ナトリウムイオンに比べてカルシウムイオンやマグネシウムイオンを選択的に吸着することができ、水の硬度を下げるために使われます。
一方、アニオン交換樹脂は、過剰な硫酸イオンや塩素イオンを除去するために利用され、特に水処理や化学分析の分野で活用されています。
最近では、より高性能な樹脂の開発が進んでおり、環境負荷としての有害物質を吸着する樹脂も開発されています。その結果、イオン交換は、単なる水処理だけでなく、様々な分野での応用が期待されています。
イオン交換の過程においては、電荷バランスとイオン交換樹脂の役割が極めて重要です。イオン交換とは、樹脂内部に固定されているイオンと水中の特定のイオンが入れ替わるプロセスであり、この反応では常に電荷の均衡が維持されます。たとえば、ナトリウムイオンが樹脂から放出される際には、同数の他の陽イオン(カルシウムイオンなど)が樹脂に吸着されます。
さらに、イオン交換には「選択性」と呼ばれる特性があり、樹脂が特定のイオンを優先的に吸着する傾向を示します。この選択性はイオンそのものの性質に加え、イオン交換樹脂の母体構造にも大きく影響を受けます。したがって、イオンおよび樹脂の特性を理解することは、反応速度や効率を正しく把握するうえで欠かせません。
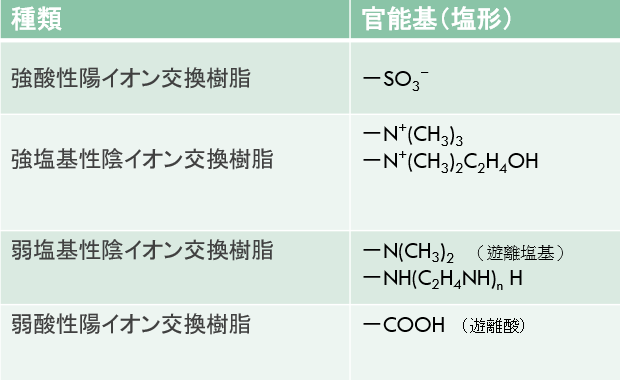
イオン交換樹脂には、通常、陰イオン交換樹脂と陽イオン交換樹脂の2つの大きなカテゴリがあります。それぞれの樹脂には、その表面に官能基と呼ばれる固定されたイオン交換サイトがあり、このサイトにてイオンの交換が行われます。この官能基が陰イオン交換樹脂と陽イオン交換樹脂でことなり、さらに電荷の強弱により強塩基、弱塩基、強酸、弱酸に大きく分けることができます。
表は官能基を示しています。官能基の種類により塩基度および酸性度がことなり、それによりイオン交換の効率、選択性および稼働pH域がことなります。
一方で交換されるイオン自体の特徴としては、一般に、価数が高いイオンほど樹脂に強く吸着される傾向があり、また同じ価数であれば原子番号の大きいイオンほど吸着性が高くなることが知られています。たとえば、強酸性陽イオン交換樹脂、強塩基陰イオン交換樹脂では、次のような順で選択性が高くなります:
H⁺ < Na⁺ < Mg²⁺ < Ca²⁺
OH⁻ < F⁻ < HCO₃⁻ < Cl⁻ < NO₃⁻ < Br⁻ < SO₄²⁻ < I⁻
これは、単価のイオン(H⁺やNa⁺)よりも、二価のイオン(Mg²⁺やCa²⁺)の方がより強く吸着されやすいことを示しています。
加えて選択性はイオンの水和半径、電荷密度などの物理化学的特性に依存します。小さくて水和が強いイオン(OH⁻、F⁻)よりも、水和が弱く分極しやすいイオン(I⁻やSO₄²⁻)の方が、樹脂に吸着されやすい傾向にあります。これは、イオン交換においては水和性の小さい大きなイオンの方が選択されやすいという性質を反映しています。
ここでは、強酸性陽イオン交換樹脂および強塩基性陰イオン交換樹脂における代表的な反応について確認していきます。これらの反応の基礎を理解することで、浄水や硬水の軟化など、実際に行われる多様なイオン交換反応をより理解しやすくなるとともに、複雑な系に対する考察や理解も一層容易になるでしょう。
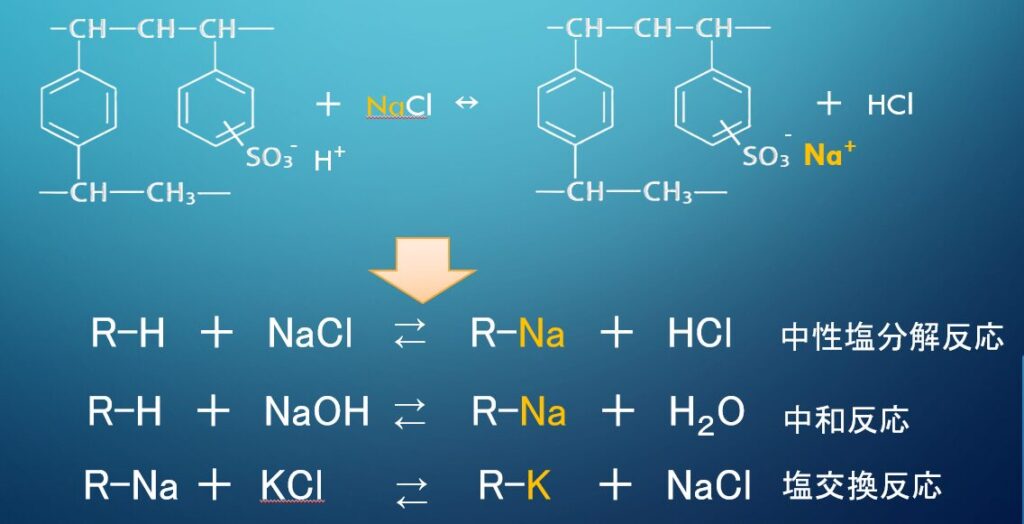
強酸性陽イオン交換樹脂は官能基としてスルホン酸基を有し、イオン交換反応は、一般的に「中性塩分解反応」「中和反応」「塩交換反応」として説明されます。特に特徴的なのは、中性塩、すなわちNaClからナトリウムイオンを吸着できる点です。この場合、樹脂はNa⁺を取り込み、代わりにH⁺を放出します。これにより強い酸性度と高いイオン交換能力を示すことがわかります。
さらに、強酸性陽イオン交換樹脂は広いpH範囲において反応が可能であり、たとえばNaOHとの反応では中和反応として表現されます。加えて、塩交換反応においては、樹脂の選択性に応じて異なるカチオンの交換が起こります。
代表的な例として、硬水中のCa²⁺やMg²⁺がNa⁺やH⁺と交換されることで、硬水の軟化処理に利用されています。この仕組みは、ボイラー給水の前処理や食品工場の水処理など、工業的にも幅広く応用されています。
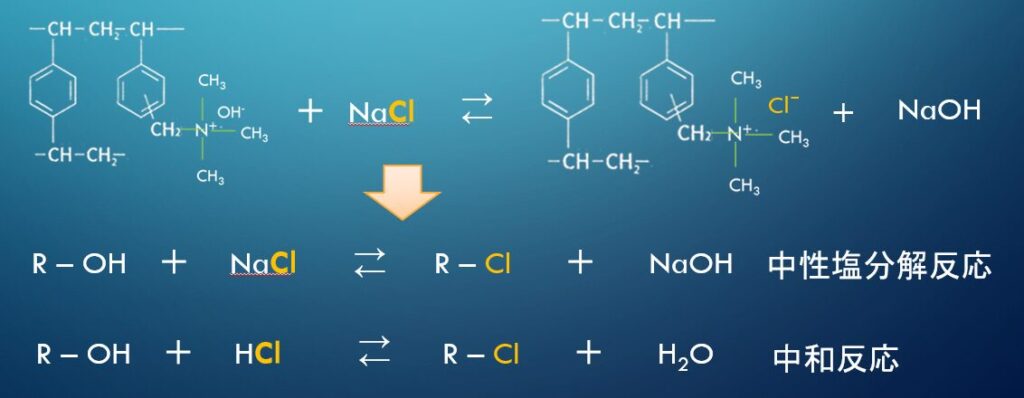
強塩基性陰イオン交換樹脂は、四級アンモニウム基を官能基として有しており、その反応は主に「中性塩分解反応」や「中和反応」として説明されます。四級アンモニウム基は広いpH範囲で常に解離しているため、酸性・アルカリ性を問わずイオン交換反応が可能です。
代表的な例として、Cl⁻やSO₄²⁻などの陰イオンを吸着し、代わりにOH⁻を放出します。この仕組みにより、陰イオン除去や純水製造に利用されるほか、SiO₂(シリカ)やNO₃⁻(硝酸イオン)など特定の陰イオン除去にも応用されています。また、工業的には電子工業用超純水の製造や食品工場における水処理など、幅広い分野で重要な役割を担っています。

純水器ボンベの家庭用レンタルを始めました。この機会に是非お試しください。
拭き取り不要 純水器のメンテナンスはいらない イオン交換樹脂の交換も不要 ボディーの美観を維持できる
数量限定によるセール価格! 無駄な自動課金はありません。

洗車キャンペーン!開催中 是非この機会にレンタル純水器を
初めての方にも手軽に純水洗車を体験していただける「レンタル純水器」をご提供しています
close